lepra, melaatsheid
te
Gerhard Armauer Hansen
(1841-1912)

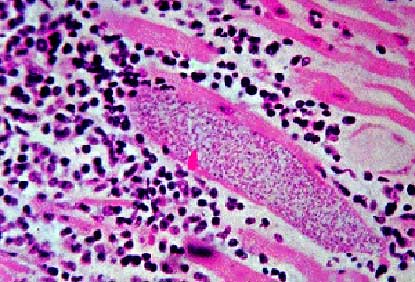
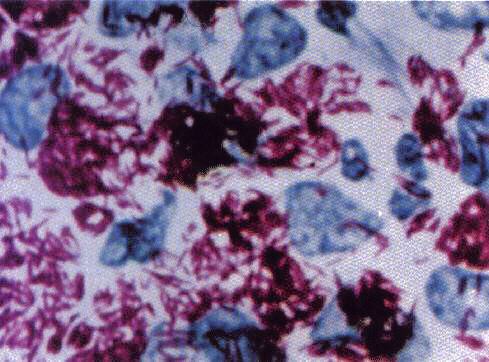
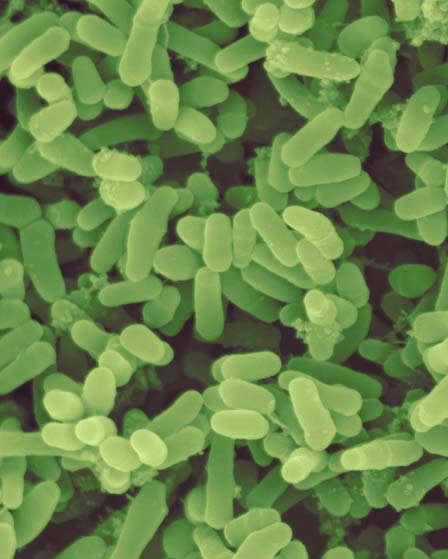
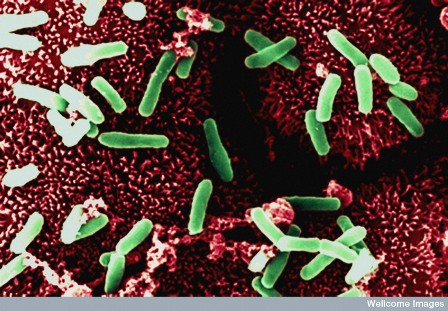
Mycobacterium leprae

n
Lepra is gevreesd vanwege de misvormingen en het daarmee samenhangende sociale stigma. In de Middeleeuwen werden lijders aan de ziekte (melaatsen) legaal dood verklaard en verstoten. Mijlpalen in de geschiedenis van lepra zijn de ontdekking van de verwekker door Hansen in 1873, de introductie van de sulfatherapie in 1941, de ontwikkeling van de techniek de bacterie te laten groeien in de voetzool van de muis in 1960, de ontdekking van groei van de bacterie in de armadillo (Dasypus novemcinctus, het negenbandig gordeldier) in 1971, en de introductie van de combinatietherapie (multi drug therapy (MDT): dapson/rifampicine/clofazimine) in 1982.
Ziekte
Verwekker
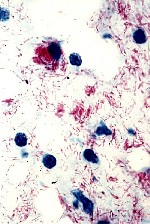
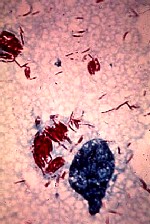
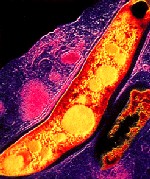
Mycobacterium leprae iseen zuurvaste staaf die veel op de tuberkelbacterie lijkt en affiniteit heeft met schwannscellen. Men is nog niet in staat de bacterie in vitro te kweken. Voor onderzoeksdoeleinden is het mogelijk de bacterie te kweken in de armadillo of de voetzool van de muis. M. leprae heeft een zeer lange delingstijd van 11 tot 13 dagen. De bacteriën zijn in lepromateuze weefselpreparaten te zien als dichte bundels voornamelijk intracellulair gelegen staafjes.
De dikke lipide-envelop beschermt de bacterie tegen veel bactericide middelen en tegen afbraak in de macrofaag.Pathogenese
Men veronderstelt dat M. leprae zich via respiratoire overdracht (druppelinfectie door multibacillaire patiënten) hematogeen verspreidt. De verwekker groeit obligaat intracellulair met name in macrofagen en schwannscellen. De expressie van de ziekte hangt af van de mate van specifieke cellulaire immuniteit tegen M. leprae. Het al dan niet ontstaan van deze immuniteit is multicausaal: de route van infectie (via de huid of via slijmvliezen), genetische factoren, én contact met andere bacteriële antigene determinanten van omgevingsbacteriën die verwant zijn aan M. leprae, spelen een rol. Bij de tuberculoïde patiënt (zie par. 2.4) is de specifieke cellulaire immuniteit sterk aanwezig, bij de lepromateuze patiënt is deze echter vrijwel afwezig.Incubatieperiode
De incubatietijd van lepra varieert van minder dan een jaar tot tientallen jaren, maar is meestal 2 tot 5 jaar voor tuberculoïde patiënten en 7 tot 12 jaar voor lepromateuze patiënten.
Ziekteverschijnselen
Of kolonisatie met M. leprae leidt tot infectie en ziekte is afhankelijk van
de weerstand van de gastheer en genetische factoren. Waarschijnlijk maakt
circa 90-95% van de geïnfecteerden de ziekte subklinisch door en herstelt
volledig.
Bij een minderheid van de geïnfecteerden (circa 5-10%) treden verschijnselen
van lepra op. Deze kunnen vanzelf genezen (75%) of leiden tot uitgebreide
polyneuropathieën en/of huidafwijkingen.
In de huid manifesteert de ziekte zich met een grote variatie van
huidlaesies. Meestal gaat het hier om één of meerdere gehypopigmenteerde of
erythemateuze laesies met sensibiliteitsverlies binnen deze laesie(s).
(Hast89)
Bij zenuwaantasting ontstaan sensibiliteitsverlies en paresen. Door het
sensibiliteitsverlies ontstaan er gemakkelijker (pijnloze) verwondingen en
ulceraties. Door paresen kunnen contracturen ontstaan van handen en voeten;
tevens kan het onvermogen ontstaan om de ogen te sluiten (lagophthalmus),
wat kan leiden tot blindheid.
Naast de huid en perifere zenuwen kunnen ook andere organen worden aangetast
zoals ogen, testis en bot (resorptie).
Het lepraspectrum wordt onderverdeeld in vijf groepen:
- tuberculoïd (TT),
- borderline tuberculoïd (BT),
- mid-borderline (BB),
- borderline lepromateus (BL),
- lepromateus (LL).
Er zijn regionale verschillen in verdeling
over de verschillende beloopvormen. Tevens bestaat er een indeterminate
lepra (I), die ofwel spontaan geneest, ofwel zich ontwikkelt tot één van de
vormen van lepra.
Indeterminate lepra(I) is een gehypopigmenteerde maculaire laesie. Het is
nog onduidelijk in welke richting van het spectrum de ziekte zich zal
begeven. Slechts de huid is aangedaan.
Bij tuberculoïde lepra (TT) bestaat een krachtige cellulaire immuunreactie
waardoor er slechts weinig ziekteverschijnselen optreden en er geen
bacteriën aantoonbaar zijn. Huidlaesies treden op in de vorm van
anesthetische en anhidrotische maculae of plaques. De laesies zijn altijd
beperkt in aantal en komen asymmetrisch voor. De zenuwtakjes in de
huidlaesie zijn aangetast. Soms is er een verdikte perifere zenuw in de
nabijheid van de huidlaesie.
De infectie is altijd sterk gelokaliseerd en nooit gedissemineerd.
Zenuwaantasting betreft zowel de motoriek als de sensibiliteit.
Patiënten met borderline lepra (de grootste groep) hebben verschijnselen van
zowel tuberculoïde als van lepromateuze lepra. Er wordt onderscheid gemaakt
in mid-borderline (BB), meer tuberculoïde (BT) en meer lepromateuze
borderline (BL). Sommigen blijven stationair, maar anderen kunnen meer
tuberculoïde of meer lepromateuze verschijnselen ontwikkelen.
Bij lepromateuze lepra (LL) is de specifieke cellulaire immuunrespons
afwezig en zijn ongeremd groeiende leprabacteriën te vinden in de huid, de
zenuwen en het reticulo-endotheliaal systeem. Ook kan er een invasie zijn
van ogen, testis, botten en slijmvliezen van mond, neus, farynx, larynx en
trachea. De huid en perifere zenuwen zijn beide, en wel symmetrisch
aangedaan. Het neustussenschot kan ulcereren en perforeren met als resultaat
een (ingezakte) 'zadelneus'. Verkorting van vingers en tenen kan optreden
ten gevolge van botresorptie. Ook kan madarosis (verlies van wenkbrauwen en
wimpers) voorkomen.
Om diagnostiek en therapiekeuze in endemische landen ook in eenvoudige
perifere kliniekjes te kunnen uitvoeren, introduceerde de WHO in 1998 een
indeling in paucibacillaire en multibacillaire vorm gebaseerd op het aantal
laesies. Paucibacillair zijn patiënten met 5 of minder laesies en
multibacillair zijn patiënten met 6 of meer laesies. Binnen de
paucibacillaire lepra wordt soms nog de ‘single lesion paucibacillary
leprosy’ (slechts één laesie) onderscheiden van de overige paucibacillaire
lepra (patiënten met 2 t/m 5 laesies). (WHO98).
Lepra heeft een sluipend beloop. De acute reacties (signalen van een
verandering in het immunologisch systeem) zijn echter zeer heftig en vormen
een medische urgentie. Er worden drie typen reacties onderscheiden:
De reversal reactie (type 1-reactie) betreft een cellulaire
hypersensitiviteit, die tot uiting komt bij een instabiele immunologische
status van de patiënt in de borderline groep. Klinisch uit zich deze reactie
in het opvlammen van de reeds aanwezige huidlaesies en het ontstaan van
nieuwe. Vaak treedt een acute neuritis op met een snel verlopend
functieverlies. Deze reactie is te beschouwen als een vertraagd type
overgevoeligheidsreactie.
Erythema nodosum leprosum (ENL, type 2-reactie) komt voor bij
multibacillaire patiënten. De meest gangbare opvatting is dat het een door
immuuncomplexen gemedieerde reactie betreft, waarbij de T-celactiviteit en
TNFα een belangrijke rol spelen.
De derde reactievorm is het Luciofenomeen: dit is zeldzaam en treedt vrijwel
alleen op bij patiënten van Mexicaanse origine. Het gaat hierbij om
pijnlijke ulcererende purpura, die na genezing een litteken achterlaten. Het
berust volgens de laatste inzichten op een cutane infarcering ten gevolge
van trombotische processen bij een ontsteking van kleine bloedvaten (venulitis).
De ziekte is zelden de directe oorzaak van de dood, maar leidt indirect tot
een lagere levensverwachting.
Verhoogde kans op ernstig beloop:
- Tijdens en enige jaren na combinatietherapie is de kans op reacties verhoogd.
- Onderbreken van de therapie geeft een grotere kans op ernstig beloop; goede voorlichting aan patiënt en familie is geboden.
- Zwangerschap. Tijdens de zwangerschap en ook in de puberteit is er sprake van hormonale veranderingen en daardoor een veranderde immunostatus. Door veranderingen in het immunologische systeem worden leprareacties in gang gezet. De type 1-acute reacties treden met name post partum op, terwijl de type 2-reacties vroeg of laat in de zwangerschap tot uiting komen. Beide typen reacties kunnen nog langdurig tijdens de lactatieperiode voorkomen. Lepra tijdens de zwangerschap kan veilig en succesvol behandeld worden met combinatietherapie.
Onderzoek tot nu toe lijkt erop te wijzen dat
hivinfectie niet leidt tot een ernstiger beloop van de lepra. (Usti06)
Immuniteit
De meeste mensen ontwikkelen een adequate afweerreactie en krijgen geen
lepra. Indien de afweerreactie onvoldoende is, treden verschijnselen van
lepra op. Het klinisch beeld dat vervolgens ontstaat, is afhankelijk van de
ontstane immuniteit. Bij tuberculoïde patiënten is de specifieke cellulaire
immuniteit sterk aanwezig, bij de lepromateuze patiënt is deze echter
vrijwel afwezig.
Zonder behandeling kan de immuniteit afnemen, waardoor de ziekte meer
lepromateuze kenmerken kan krijgen (zogenaamde downgrading). Als gevolg van
type 1-reactie kan de ziekte ook meer tuberculoïde kenmerken krijgen
(upgrading). De acute reacties worden beschouwd als een signaal van een
verandering in het immunologische systeem. De precieze achtergrond van de
veranderingen in de immuniteit is nog niet opgehelderd. Men veronderstelt
dat het doormaken van lepra niet beschermend werkt tegen het opnieuw krijgen
van lepra.
Diagnostiek
Microbiologische diagnostiek
Het aantonen van de bacterie in een preparaat van huidvocht (skinsmear) of huidbiopt. (WHO98) Wade-Fite- of ziehl-neelsenkleuring zijn technieken die gebruikt worden bij lepradiagnostiek.
Een PCR voor het opsporen van bacterieel DNA in neuswatten, biopten en skinsmears is mogelijk maar nog nauwelijks gebruikt bij de lepradiagnostiek. (Brit04)
Overige diagnostiek
Kliniek
Diagnostiek bij lepra berust op de aanwezigheid van één of meer van de volgende criteria (bij iemand die nog geen volledige behandeling voor lepra heeft gehad):
- gehypopigmenteerde of erythemateuze huidafwijking(en) met verlies van het fijne tastgevoel (dit kan getest worden door middel van een tot draadje gedraaid wattenbolletje);
- betrokkenheid van perifere zenuwen, aangetoond door verdikte zenuwen en verlies van sensibiliteit, motorische uitval of autonome uitval;
- het aantonen van de bacterie in een preparaat van huidvocht of huidbiopt (skinsmear) met behulp van Wade-Fite- of ziehl-neelsenkleuring. (WHO98).
Biopsie
Histopathologisch onderzoek van een huidbiopt, en zonodig van een zenuwbiopt in geval van verdenking op zogenaamde neurale lepra, is in Nederland een standaard diagnostische procedure.
Serologie
Serologie wordt momenteel (nog) niet veel gebruikt bij de diagnostiek van lepra. Wel wordt serologie gebruikt als hulpmiddel bij de classificatie van een nieuwe leprapatiënt (voor behandelingsdoeleinden) én het screenen van contacten van leprapatiënten om contacten met verhoogd risico op lepra op te sporen en eventueel (tijdig) te behandelen. (Bühr03)
Er is een ELISA beschikbaar voor het aantonen van antistoffen tegen de terminale suikercomponent van het M. leprae-specifieke fenolische glycolipide-I. Deze antistoffen zijn aantoonbaar bij 90% van de patiënten met onbehandelde lepromateuze lepra, maar slechts bij 15-40% van de patiënten met paucibacillaire lepra, alsmede bij 1-5% van de gezonde controlepersonen. (Brit04)
Ook is er een laterale flow sneltest beschikbaar die binnen 10 minuten een uitslag geeft. Deze test is gebaseerd op dezelfde antistoffen tegen de terminale suikercomponent van het M. leprae-specifieke fenolische glycolipide-I en laat resultaten zien die vergelijkbaar zijn met de ELISA-test. (Bühr03).
Besmetting
Reservoir
De mens is het enige reservoir van betekenis. Multibacillaire leprapatiënten gelden als de belangrijkste bron. Bij armadillo’s in Noord-Amerika komt natuurlijke overdracht voor. Bij de mangabeyaap (Nigeria) en de chimpansee (Sierra Leone) is lepra gevonden. Er zijn geen aanwijzingen dat deze dieren een belangrijke besmettingsbron zijn voor de mens.Besmettingsweg
Respiratoire overdracht via een druppelinfectie door multibacillaire patiënten wordt gezien als de belangrijkste besmettingsweg. Er is echter geen formeel bewijs dat dit ook daadwerkelijk zo is. Bacteriën dringen het lichaam vooral via de bovenste luchtwegen binnen (mogelijk via slijmvlieslaesies). Ook via huidulcera en andere verwondingen kunnen patiënten bacteriën verspreiden. De overdracht via moedermelk en bijtende insecten is als mogelijkheid beschreven.Besmettelijke periode
Het is onduidelijk vanaf welk moment een (onbehandelde) leprapatiënt mogelijk besmettelijk is.
Binnen 3 dagen na de start van therapie met rifampicine is een patiënt niet meer besmettelijk.Besmettelijkheid
Lepra is gemakkelijk overdraagbaar getuige de hoge seroprevalentie die gevonden wordt in hoogendemische gebieden. Daar vindt overdracht met name plaats in het gezin, maar in mindere mate ook daarbuiten naar buren, buurtgenoten en mogelijk ook andere sociale contacten. (Moet06) De kans om geïnfecteerd te raken, is bij gezinsleden van lepromateuze patiënten vier keer hoger dan bij die van tuberculoïde patiënten. (Hast89).
Desinfectie
M. lepraeoverleeft in gedroogd neusslijm in een warm en vochtig klimaat tot
9 dagen. Rond het vriespunt kan de bacterie 2 weken overleven, hij overleeft
bevriezing tot -80°C. Onder gunstige omstandigheden kan de bacterie veel
langer overleven; 14-30 dagen is aangetoond. Verhitting tot 45°C gedurende 1
uur overleeft de bacterie niet, maar antigene activiteit blijft bestaan tot
temperaturen boven de 100°C.
Verspreiding
Risicogroepen
In endemische gebieden: huisgenoten en
daarmee vergelijkbare contacten van een persoon met lepra.
Lepra wordt met name gezien in de armere bevolkingsgroepen in laag- en
middeninkomenlanden.
Verspreiding in de wereld
Sinds 2001 lijkt de incidentie van lepra wereldwijd langzaam af te nemen. In
2005 zijn er wereldwijd ongeveer 296.000 nieuwe leprapatiënten
gediagnosticeerd. (WHO06)
De prevalentie is de afgelopen 20 jaar afgenomen van 5,2 miljoen (1985) tot
ongeveer 222.000 geregistreerde gevallen begin 2006. (WHO05) Deze
prevalentiedaling is het gevolg van de introductie van de combinatietherapie
en de hiermee gepaard gaande gewijzigde registratie. Sinds de introductie
van de combinatietherapie worden patiënten namelijk niet langer levenslang
behandeld en geregistreerd, maar alleen gedurende de periode van de
combinatietherapie. Ook zijn lepraregisters opgeschoond en is ná de
introductie van de combinatietherapie de behandelduur hiervan nog weer
verder ingekort. Dit alles dus met enorme prevalentiedalingen tot gevolg. De
prevalentie en incidentie wisselen sterk per regio.
Voorkomen lepra in de wereld (2005) (WHO05):
- Zuidoost-Azië
0,79 /10.000 inwoners
11,99/100.000 inwoners - (Tropisch) Afrika
0,63/10.000 inwoners
6,48/100.000 inwoners - Delen van Midden- en Zuid-Amerika
0,39/10.000 inwoners
5,00/100.000 inwoners
In 2005 kwam 82% van alle nieuwe
lepragevallen uit een zestal landen: India, Brazilië, Indonesië, D.R. Congo,
Bangladesh en Nepal (in afnemend (absoluut) aantal nieuw gevonden gevallen).
India vertegenwoordigt hierin het grootste deel met 54% van de wereldwijd
nieuw gevonden gevallen. (WHO06)
Ook de verdeling van beloopvormen wisselt per regio. Deels berust dit op
verschillen in definities voor de classificatie, deels op werkelijke
verschillen. Het percentage lepromateuze lepra is over het algemeen hoger in
Zuidoost-Azië en Amerika (meer dan de helft) dan in Afrika en India (minder
dan de helft).
Voorkomen in Nederland
Lepra is in Nederland een importziekte. In de periode 1991-1997 werden er 68
gevallen van lepra gemeld bij GGD’en (60% mannen, 40% vrouwen). (Post94)
Aangezien lepra per 1 april 1999 niet meer meldingsplichtig is, zijn er geen
exacte recentere incidentiecijfers voor Nederland bekend. Echter, op basis
van de aantallen nieuwe patiënten die in de gespecialiseerde centra in
Nederland gezien zijn in de periode 2000 – 2006, is de schatting dat er
jaarlijks circa 5-10 nieuwe patiënten gediagnosticeerd worden in Nederland.
Behandeling
In verband met het belang van (tijdige) herkenning en behandeling van
complicaties is de behandeling en begeleiding van leprapatiënten binnen
Nederland in een gespecialiseerd centrum (zie par. 10.2) geboden. De
behandeling van lepra is langdurig en kan onderscheiden worden in
chemotherapeutische behandeling en de revalidatie en/of rehabilitatie van
reeds aanwezige invaliditeit.
Chemotherapeutische behandeling
Door de toename van resistentie voor dapson (4,4’-diamino-diphenylsulphone:
DDS) is combinatietherapie van dapson, rifampicine en clofazimine momenteel
de gangbare therapie.
De WHO beveelt in geval van paucibacillaire lepra aan om binnen een periode
van maximaal 9 maanden 6 maanden therapie te geven van dapson 1dd 100 mg met
daarbij ook steeds één dosis rifampicine 600 mg per maand onder supervisie.
Bij multibacillaire lepra is het WHO-advies: dapson 1dd 100 mg en
clofazimine 1dd 50 mg samen met rifampicine 600 mg eenmaal per maand en
clofazimine 300 mg eenmaal per maand onder supervisie. Voor adequate
therapie moeten de geneesmiddelen gedurende 12 maanden worden ingenomen. Dit
regime dient binnen 18 maanden plaats te vinden. (WHO00)
In verband met de langdurige behandeling is ondersteuning van de
therapietrouw van groot belang.
NB. Bacteriën kunnen tot 20 jaar na therapie in granulomen gevonden worden;
ze zijn dood en worden door het lichaam opgeruimd. Op sommige plaatsen
kunnen soms intacte (zogenaamde ‘dormant’ bacteriën) gevonden worden.
Een recidief wordt behandeld met dezelfde combinatietherapie. De acute
reacties vereisen directe behandeling met prednison. Bij ENL is Thalidomide
(Softenon®; cave teratogeniciteit!) effectief gebleken.
|
Gerhard Armauer
Hansen
Lepra in Noorwegen
Erfelijk of besmettelijk |
|
Het duurde echter nog lang voor zijn ontdekking op juiste waarde werd geschat: Danielssen, in die tijd nog steeds verbonden aan hetzelfde lepraziekenhuis, bleef ervan overtuigd dat lepra erfelijk bepaald was. Hansen zelf moest voor de rechter zijn experimenten met leprapatiënten verdedigen en een Duitse student claimde dat hij de ontdekker was van de bacil.
Erkenning
In 1909, tijdens het 2e Internationale Lepra Congres in Bergen bleken alle
lepradeskundigen er inmiddels wél van overtuigd dat lepra besmettelijk was
en werd Hansen als officiële ontdekker van de lepra-bacil erkend.